千葉大学大学院薬学研究院の殿城亜矢子講師と伊藤素行教授、千葉大学真菌医学研究センターの高橋弘喜准教授の研究グループは、脳内で一酸化窒素によって活性化される可溶性グアニル酸シクラーゼ注1)が加齢に伴い増加することが、認知症の発症リスクを上昇させる一つの要因であることを明らかにしました。本研究成果により、認知症に対する新薬開発や新たな生体内リスクマーカー注2)の発見などが期待されます。
本研究成果に関する論文は、2022年8月13日にAging Cellに掲載されました。
■ 研究の背景
超高齢化社会が進行している日本では、認知症の患者数が増え続けていますが、その発症メカニズムには多くの不明な点があります。認知症の発症リスクを上昇させる最大の要因は「加齢」です。加齢に伴う脳内の遺伝子発現の変化が認知症の発症要因となっている可能性が考えられますが、それらを網羅的に探索する研究は多大な労力と時間がかかるため、あまり行われてきませんでした。
認知症を含む加齢性記憶障害は、ヒトだけでなく、マウス、ショウジョウバエ、線虫など多くのモデル動物でも共通してみられる現象です。同研究グループは、寿命が短いため老齢個体を容易に得ることができるショウジョウバエをモデル動物として用いました。ショウジョウバエは、匂いと電気刺激を同時に与えられると、その匂いを電気刺激と関連付けて学習し、一定時間記憶することができますが、老化したショウジョウバエでは記憶する能力が低下します。同研究グループはこのようなモデルを用いて、加齢に伴い脳内で発現量が変化することによって記憶低下の原因となる遺伝子を網羅的に探索することとしました。
■ 研究成果
同研究グループは、遺伝子の発現量を解析する手法のRNAシーケンス注3)を用いて、ショウジョウバエ脳内で加齢に伴い発現量が変化する遺伝子を抽出しました。さらに、データベースとの比較解析を駆使して、記憶低下の原因となる候補遺伝子を絞り込みました。それぞれの候補遺伝子の発現量を脳内で改変したショウジョウバエを作製し、それらの記憶能力を測定しました。その結果、一酸化窒素(NO)によって活性化される可溶性グアニル酸シクラーゼ(sGC)の発現量が加齢に伴い増加し、sGCの発現量を脳内で低下させると記憶が上昇することが明らかになりました。
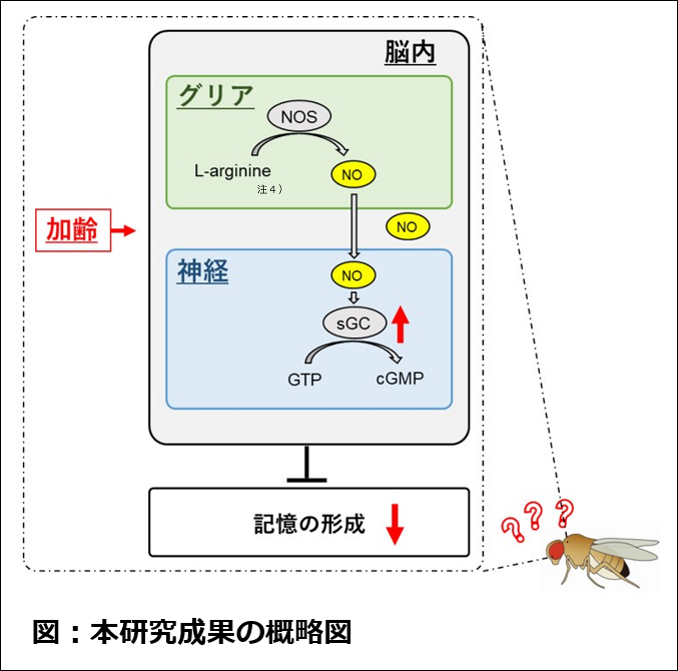
具体的には、一部の神経細胞でsGCの発現量を抑制させたショウジョウバエや、sGCを阻害する薬剤を投与したショウジョウバエでは、加齢による記憶低下が改善しました。さらに、脳内の神経細胞の周囲に存在するグリア細胞で、NOを合成する酵素であるNO合成酵素(NOS)の発現量を抑制させたショウジョウバエや、NOSを阻害する薬剤を投与したショウジョウバエでも、記憶低下が改善しました。
これらのことより、加齢に伴いNOやsGCに関連する経路が活性化することが、記憶の低下を引き起こす一つの原因となることが示唆されました。
■ 今後の展望
NOやsGCに関連する経路は、ヒトを含めた哺乳類でも同様に機能しています。今後は、NOやsGCに関連する経路が加齢に伴い活性化するメカニズムや記憶を低下させるメカニズムのさらなる解明が期待されます。また、本研究で明らかになったことが、認知症に対する新薬開発や新たな生体内リスクマーカーの発見に繋がることが期待されます。
■ 用語解説
注1)可溶性グアニル酸シクラーゼ: NOにより活性化されると、グアノシン三リン酸(GTP)から環状グアノシン一リン酸(cGMP)の生成を触媒する酵素。
注2)リスクマーカー:疾患の発症リスクと相関し、発症リスクを予測できる特定の物質や遺伝子。
注3)RNAシーケンス: 遺伝子の塩基配列を高速に解読できる次世代シーケンスを用いて、取得した情報をデータ解析することで、遺伝子の発現量を網羅的に解析できる手法。
注4)L-arginine:アミノ酸の一つであるL-アルギニン。NO合成酵素により、L-アルギニンからNOが合成される。
■ 論文情報
論文タイトル:Nitric oxide-soluble guanylyl cyclase pathway as a contributor to age-related memory impairment in Drosophila.
著者:Ayako Tonoki, Saki Nagai, Zhihua Yu, Tong Yue, Sizhe Lyu, Xue Hou, Kotomi Onuki, Kaho Yabana, Hiroki Takahashi, Motoyuki Itoh
雑誌名:Aging Cell
DOI:https://doi.org/10.1111/acel.13691
■研究支援
本研究は、日本医療研究開発機構(AMED)革新的先端開発支援事業「全ライフコースを対象とした個体の機能低下機構の解明」(JP19gm6110024)、科学研究費補助金(JP16H06279、JP18K19370、JP21H02621)、内藤記念科学振興財団、武田科学振興財団の支援により実施されました。









